Lupus : une maladie auto-immune aux multiples visages
Le lupus est une maladie auto-immune chronique et diffuse à tout le corps. Elle se manifeste le plus souvent par des lésions au niveau de la peau et des douleurs articulaires, mais le lupus peut également atteindre des organes comme le rein, le cœur, le cerveau… Les progrès thérapeutiques ont té importants ces dernières années.
Par le Dr Jean-Paul Marre, rhumatologue, CHU Pitié-Salpêtrière, Paris
Des mots pour les maux
Le lupus érythémateux disséminé est une maladie auto-immune chronique, de la famille des connectivites. Les connectivites regroupent des maladies systémiques, c’est-à-dire touchant plusieurs organes ce qui est à l’origine d’une présentation très diversifiée.
Le lupus, comme les connectivites, est caractérisé par des auto-anticorps qui sont dirigés contre différentes parties du corps. Ces anticorps jouent donc un rôle important dans l’apparition des atteintes d’organes.
Le risque est l’évolution vers une détérioration, progressive et parfois brutale, de différents organes et, en particulier, le rein, le cœur et le cerveau.
Le traitement est chronique et basé sur les anti-inflammatoires, les corticoïdes et les médicaments qui visent à réduire l’auto-immunité, les immuno-modulateurs. Plus récemment, des biothérapies ont montré leur intérêt dans certaines formes de lupus.
Qu'est-ce que le lupus ?
Le lupus est une maladie chronique, d’origine auto-immune, c’est-à-dire qu’elle s’explique par un dérèglement du système de l’immunité. Celui-ci est normalement chargé de défendre notre corps contre les agressions externes et internes, mais dans le cas du lupus, l’activité anormale des cellules de défense de notre corps, les lymphocytes, entraînent une agression de différents composants de tous les organes de notre corps : la peau, les articulations, le rein, le cœur, le cerveau…
L’hyperactivité du système immunitaire dans le lupus, qui se manifeste aussi par différents auto-anticorps, a vraisemblablement pour origine de multiples facteurs, même si les causes exactes restent inconnues.
Du fait de la diversité des causes et de la grande variété des atteintes possibles (maladie systémique), l’expression de la maladie sera différente pour chaque individu. Elle peut être exclusivement cutanée (sans aucun risque d’atteinte ultérieure d’un organe vital), ou plus diffuse et touchant plusieurs organes, ce qui peut conduire à des atteintes sévères si la maladie n’est pas bien traitée.
En effet, l’absence de traitement adapté et surtout bien suivi, et les formes diffuses de la maladie lupique peuvent aboutir à des défaillances de différents organes, et en particulier le rein, le cœur, le cerveau... Cette grande diversité dans la maladie est la raison pour laquelle les médecins cherchent à développer une prise en charge et un traitement adaptés au plus près du profil de chaque malade.
Quelles sont les causes du lupus ?
Le lupus est une maladie auto-immune qui ne peut pas être rattachée à une seule cause. Sa cause exacte est inconnue et son origine tient probablement plus à l’association de plusieurs facteurs et d’un terrain génétique prédisposant (maladie multifactorielle).
Parmi les facteurs prédisposant, les facteurs immunogénétiques sont les plus connus : le risque d’avoir une maladie lupique chez deux vrais jumeaux est 4 fois plus important que chez les faux jumeaux. Le lupus n’est, en effet, pas associé à une anomalie majeure d’un seul gène (comme dans l’hémophilie), mais ce sont différentes particularités génétiques qui, associées, prédisposent à développer la maladie (« maladie multigénique »). Ces petites différences génétiques des gènes de l’immunité sont appelées « polymorphismes ». On retrouve donc une prédisposition génétique au lupus associée à certains groupes HLA et à certains gènes, mais aucune anomalie, prise isolément, ne suffit pour provoquer la maladie.
Les facteurs d’environnement susceptibles de participer au déclenchement d’un lupus sont nombreux mais, là encore, aucun ne peut à lui seul déclencher la maladie. Il faut certainement plusieurs facteurs d’environnement (associés à des vulnérabilités génétiques du système immunitaire) pour provoquer la maladie. Les facteurs d’environnement les plus connus sont des virus, comme les virusceux de la mononucléose infectieuse (virus d’Epstein-Barr), et différents médicaments (comme la procaïnamide, la quinidine, l’hydralazine…), ainsi que des facteurs toxiques. D’autres facteurs plus connus, comme les rayons ultraviolets (du soleil) et les hormones des femmes (estrogènes), sont sans doute plus importants. En revanche, il n’y a pas de métier connu comme favorisant l’apparition d’un lupus systémique. La responsabilité de certains produits utilisés pour les teintures capillaires avait été évoquée dans le passé, mais cela a été éliminé depuis.
Pourquoi le lupus touche surtout les femmes ?
Le lupus, comme la plupart des maladies auto-immunes, touche beaucoup plus souvent les femmes que les hommes (9 femmes pour un homme). Cette prédominance féminine n’est pas très claire et est probablement en rapport avec de nombreuses causes, même si elle peut s’expliquer du fait des différences hormonales ou des différences génétiques.
La cause hormonale de cette prédominance féminine de la maladie est l’explication la plus traditionnellement avancée. Les hormones des femmes et, en particulier les estrogènes, favorisent globalement l’excès d’immunité observé dans le lupus. Cela explique que la maladie puisse s’aggraver pendant la grossesse, lors de la prise de contraceptifs hormonaux à base d’estrogènes ou lors du traitement hormonal substitutif après la ménopause.
Le chromosome X, dont les cellules féminines portent deux exemplaires (XX), alors que les cellules masculines n’en portent qu’un (XY), est un chromosome sur lequel on trouve des gènes importants de notre système immunitaire. Il a été démontré qu’une femme lupique exprimerait différemment les gènes de l’immunité portés par le chromosome X, ce qui pourrait favoriser une hyperactivité du système immunitaire.
Le lupus peut-il être secondaire à l’usage de certains médicaments ?
Un lupus peut apparaître suite à la prise de certains médicaments. On considère alors que le lupus a été « induit » par la prise de ces médicaments et on parle de « lupus induit ». Ce profil de maladie induite se manifeste par un profil auto-immun différent avec des auto-anticorps différents.
Parmi ces médicaments, on retiendra la doxycycline (antibiotique fréquemment prescrit contre certaines infections et l’acné), certains antituberculeux, certains bêtabloqueurs (médicaments antihypertenseurs), certains antiépileptiques (carbamazépine), les anti-TNF.
La liste des médicaments potentiellement inducteurs est très longue et elle est régulièrement remise à jour, mais il est parfois difficile d’être certain du caractère vraiment inducteur de ces médicaments pour le lupus. Dans certains cas, l’arrêt du médicament « inducteur » n’entraîne pas, en effet, la disparition de la maladie lupique.
Le lupus chez la mère peut-il se transmettre à l’enfant ?
Le lupus n’est pas une maladie héréditaire, même s’il peut exister une prédisposition familiale aux maladies auto-immunes. En revanche, un « lupus néonatal » est une complication de la maladie lupique, lupus de la mère qui va affecter le fœtus ou le nouveau-né. Cette complication est toujours associée à la présence de certains auto-anticorps chez la mère : les anti-SSA (anti-Ro) ou SSB (anti-La) la mère.
Ces anticorps sont capables de passer de la mère vers le fœtus, en traversant la barrière du placenta, et ils peuvent attaquer certains organes de l’enfant. Il peut, en particulier, se produire une éruption chez le nouveau-né, qui ressemble au lupus cutané et, plus grave, mais plus rare, un ralentissement de la conduction électrique dans le cœur du fœtus, appelé « bloc auriculo-ventriculaire congénital » : 1 % des enfants de mères lupiques porteuses d’anticorps anti-SSA courent ce risque. Ce bloc de conduction des influx nerveux dans le cœur ralentit les battements du cœur de l’enfant et expose à un arrêt cardiaque. On peut observer, plus rarement, une maladie du foie ou des troubles neurologiques.
A la naissance, les anticorps anti-SSA de la mère sont progressivement éliminés et l’éruption cutanée va régresser, en revanche, le ralentissement de la conduction électrique du cœur peut persister, ce qui peut conduire à appareiller le cœur de l’enfant à la naissance. Lors d’une grossesse lupique, la présence des anticorps anti-SSA justifie une surveillance rapprochée du cœur de l’enfant par échographie.
A côté du lupus néonatal, il peut exister un lupus chez l’enfant mais ces formes pédiatriques sont rares : elles représentent environ 5 % des lupus. Ce lupus de l’enfant est souvent sévère, avec une atteinte rénale plus fréquente que dans la forme de l’adulte. Il serait moins nettement associé au sexe féminin.
Quand le lupus expose-t-il à un risque de phlébites et de thromboses ?
Le syndrome des anticorps anti-phospholipides (SAPL) est une maladie auto-immune qui peut être associée au lupus (SAPL secondaire). Le SAPL est caractérisé par la présence d’anticorps dirigés contre les phospholipides. Les phospholipides sont des constituants des membranes des cellules, dont les cellules des parois des vaisseaux sanguins. En interagissant avec ces membranes des parois des vaisseaux, ces anticorps peuvent activer la coagulation et entraîner l’apparition de caillots de sang (thromboses). La particularité de ces caillots est qu’ils peuvent se former aussi bien dans les veines (phlébites à répétition), que les artères (thromboses artérielles). Chez la femme enceinte, ces anticorps peuvent boucher les vaisseaux du placenta, diminuer ainsi les échanges entre la mère et son enfant, et provoquer une fausse-couche.
La formation de caillots de sang peut se produire dans tous les vaisseaux du corps : artères du cerveau, du rein, du cœur ou veines des membres, du cou, du foie… En fonction du type et de l’endroit anatomique où le vaisseau est bouché, les symptômes seront différents ce qui complique le diagnostic. Mais on peut avoir des anticorps anti-phospholipides, sans qu’ils augmentent pour autant le risque de caillots sanguins.
Le SAPL peut également être isolé et on parle alors de SAPL primaire.
Le lupus peut-il s’associer à d’autres maladies auto-immunes ?
D’autres maladies auto-immunes peuvent s’associer au lupus, probablement en raison d’un terrain génétique commun.
Le syndrome de Gougerot-Sjögren peut s’associer au lupus, dans environ 30 % des cas. Il s’agit d’une maladie auto-immune qui touche surtout les glandes exocrines et qui se manifeste principalement par une sécheresse de la bouche et/ou des yeux.
Le syndrome des anticorps anti-phospholipides (SAPL), qui se caractérise sur le plan clinique par l’apparition des caillots de sang (thromboses) (caillots de sang) au niveau des artères ou des veines est souvent associé au lupus également.
Enfin, d’autres maladies auto-immunes systémiques, comme les myopathies inflammatoires, la polyarthrite rhumatoïde ou la sclérodermie, peuvent être associées au lupus.
Quand doit-on évoquer un lupus ?
Le lupus se manifeste différemment selon les individus et souvent les signes avant-coureurs sont trop peu spécifiques pour faire évoquer un lupus : fièvre, fatigue, douleurs articulaires ou musculaires... La présentation la plus répandue de lupus est une inflammation qui touche la peau, les articulations, le rein, le cœur et le cerveau. Les signes n’apparaissent pas tous en même temps et s’associent progressivement, selon une chronologie qui peut être propre à chaque malade.
La maladie débute souvent par une atteinte de la peau. Il peut s’agir d’une simple réaction exagérée au soleil, même après une exposition modérée (« photosensibilité »), mais l’atteinte la plus caractéristique se fait sur le visage avec une plaque rouge et inflammatoire dont le contour ressemble à celui d’ailes de papillon (érythème en vespertilio) ou d’un loup de Carnaval. Parfois, ce sont simplement des plaques rouges arrondies (lupus discoïde). Une perte de cheveux (« alopécie »), sur une partie ou l’ensemble du cuir chevelu, peut aussi faire évoquer la maladie.
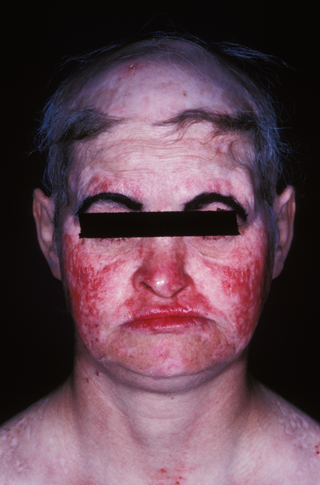
© Inserm/Guillevin, Loïc
Serimedis.inserm.fr
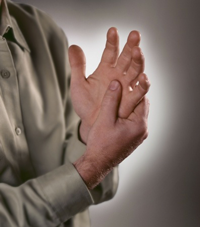
L’apparition d’un syndrome de Raynaud peut aussi être un des premiers signes de la maladie. Il s’agit d’un trouble paroxystique de la circulation du sang dans les extrémités (doigts, pieds). Il se traduit par une décoloration des doigts, ceux-ci devenant tout blancs, souvent en réaction au froid. Le retour du sang dans les extrémités se traduit par une phase de recoloration où les doigts sont successivement bleus, puis rouges, avant de reprendre leur couleur normale. La décoloration s’accompagne généralement de douleurs des doigts.
Dans d’autre cas, ce sont des douleurs articulaires qui inaugurent la maladie : il s’agit de douleurs des articulations qui vont gêner le sommeil et s’accompagner d’un enraidissement des articulations touchées le matin. Ces douleurs vont aussi s’estomper, au moins en partie, lors de l’effort : ce sont des douleurs que les médecins caractérisent comme inflammatoires. Elles peuvent s’accompagner d’un gonflement articulaire et prendre alors l’aspect d’une polyarthrite. Mais, à la différence de la polyarthrite rhumatoïde, cette arthrite ne s’accompagne pas de destructions du cartilage et des surfaces osseuses articulaires, même si dans certaines formes, une déviation des doigts peut être observée (« coup de vent cubital »).
Parfois, la maladie se révèle par une inflammation des enveloppes du cœur (péricardite) ou du poumon (pleurésie), ou par une atteinte des reins (atteinte glomérulaire) avec fuite de protéines et de globules rouges dans les urines. Celles-ci se traduisent par de volumineux œdèmes des membres inférieurs, en particulier le soir.
Mais le lupus peut toucher tous les organes et une grande diversité de symptômes peut ainsi être observée. D’autres signes peuvent ainsi plus rarement inaugurer la maladie : atteinte du cerveau, c’est-à-dire une épilepsie, des troubles psychiatriques (« psychoses »), des troubles de la motricité et de la sensibilité, atteinte digestive (pancréatite, hépatite...), atteinte cardiovasculaire (atteinte des valves du cœur, inflammation du cœur à type de myocardite, une thrombose artérielle ou veineuse (phlébite).
Les signes sont plus ou moins sévères en fonction des malades et des phases de la maladie et peuvent faire évoquer d’autres maladies. Du fait de sa propension à mimer d’autres maladies, le lupus est donc un défi pour les médecins.
Comment faire le diagnostic de lupus ?
Le lupus est une maladie auto-immune qui peut se manifester par une atteinte des différents organes (« maladie systémique »). Le diagnostic de lupus repose donc sur un ensemble de signes cliniques et biologiques qui peut varier d’un patient à l’autre. Certains de ces signes sont très évocateurs de la maladie (comme certaines lésions cutanées) et d’autres le sont moins car ils existent dans d’autres maladies auto-immunes (arthrites, péricardites…).
La plupart du temps, les différents organes concernés ne sont pas tous touchés en même temps, mais cela amène à des présentations très variables de la maladie. Tous les signes ne sont donc pas présents en même temps et au même moment. Le médecin devra donc s’intéresser à l’histoire du patient en l’interrogeant sur ses anciennes maladies et ses antécédents familiaux pour poser un diagnostic.
Le diagnostic peut être évident à la phase d’état de la maladie où il est le plus souvent porté par le médecin sur l’association d’au moins 4 signes parmi une liste de 11 dont l’intérêt a été validé dans de nombreuses conférences de consensus. Mais ces critères sont des critères de classification et ne sont pas suffisants pour porter le diagnostic au début de la maladie où le diagnostic est plus subtil.
Pour faire le diagnostic de lupus devant ces premiers signes cliniques, une prise de sang peut être très contributive si elle est associée à un signe très évocateur comme les lésions cutanées : pratiquement tous les malades à ce stade ont une baisse des globules blancs (leucopénie) ou des plaquettes (thrombopénie), mais c’est la recherche des auto-anticorps qui sera décisive : la présence d’anticorps antinucléaires, à titre élevé (c’est-à-dire à un titre supérieur ou égal à 1/320) sera particulièrement intéressante surtout si elle s’associe à la présence d’anticorps anti-ADN ou d’anti-Sm.
C’est l’association de plusieurs signes témoignant d’une atteinte de différents organes et d’un état auto-immun, objectivé par des examens du sang, qui permettra de poser un diagnostic au début. Pour établir un diagnostic avéré et reconnu au niveau international, la communauté scientifique médicale a établi une liste de 11 critères parmi lesquels au moins 4 sont nécessaires pour établir un diagnostic de lupus :
- Rash malaire
- Lupus discoïde
- Photosensibilité
- Ulcérations orales ou nasopharyngées
- Arthrite non érosive touchant au moins 2 articulations périphériques
- Pleurésie ou péricardite
- Protéinurie > 0,5 g/jour ou cylindrurie
- Convulsions ou psychose
- Anémie hémolytique
- Leucopénie < 4000/µl constatée à 2 reprises
- Lymphopénie < 1500/µl constatée à 2 reprises
- Thrombopénie < 100 000/µl en l'absence de drogues cytopéniantes
- Anticorps anti-ADN natif
- Anticorps anti-Sm?Sérologie syphilitique dissociée constatée à 2 reprises en 6 mois, ou anticoagulant circulant de type lupique ou anticorps anticardiolipine (IgG ou IgM)
- Titre anormal d’anticorps antinucléaires en l'absence de drogues inductrices.
Quels sont les examens nécessaires pour le diagnostic de lupus ?
Le diagnostic de lupus dépend beaucoup des premiers signes de la maladie. Les examens sont réalisés par le médecin, d’une part pour éliminer une maladie qui ressemblerait au lupus, d’autre part, pour affirmer si possible le diagnostic, et enfin, pour évaluer l’atteinte des organes concernés par la maladie afin d’ajuster au mieux le traitement.
Les examens les plus utiles au diagnostic de lupus sont les examens de sang et les examens immunologiques. Le médecin recherche en premier une diminution des différents globules dans le sang : baisse des globules rouges (anémie hémolytique), baisse des globules blancs (lymphopénie et/ou neutropénie), baisse des plaquettes (thrombopénie auto-immune).
Il est aussi fondamental de rechercher une souffrance des reins par l’analyse de la fonction rénale (mesurée par la créatinine) et l’analyse des urines qui permet de savoir s’il y a une atteinte inflammatoire qui touche le système de filtration du sang (glomérule). Si cette inflammation existe, les urines vont contenir des protéines (notamment de l’albumine = albuminurie), mais aussi des globules blancs (leucocyturie) et des globules rouges (hématurie). Ces anomalies rénales ne sont pas spécifiques du lupus, mais sont indispensables à rechercher quand on évoque cette maladie car elles ont une importance capitale pour le pronostic et l’orientation du traitement.
La recherche d’anomalie de la fonction du foie (transaminases, phosphatases alcalines) est surtout utile pour éliminer une autre maladie (virus), car il n’y a pas d’atteinte spécifique du foie dans le lupus. Enfin, il est utile de rechercher sur l’électrophorèse du sang un taux élevé d’immunoglobulines (hypergammaglobulinémie), qui traduit l’activation du système immunitaire
Les examens immunologiques dans la prise de sang sont les examens les plus importants pour affirmer le diagnostic avec la mise en évidence dans le sang d’anticorps antinucléaires et la caractérisation de leur type (anti-ADN natifs, anti-Ro/SS-A et La/SS-B, Sm, RNP,…). Dans les formes diffuses, la recherche d’une activation du système du complément est importante et elle se traduit par sa baisse dans le sérum (hypocomplémentémie).
Ces examens immunologiques doivent comporter systématiquement la recherche d’anticorps antiphospholipides pour rechercher un syndrome des anti-phospholipides. Ceux-ci sont des auto-anticorps qui « épaississent » le sang, entraînant un risque de coagulation dans les veines (appelée phlébite) ou dans les artères (thrombose).
D’autres examens peuvent être utiles en fonction des signes que présente le malade pour compléter la démarche diagnostique ou évaluer le retentissement de la maladie sur un organe.
Une biopsie cutanée (sous anesthésie locale) peut être nécessaire pour confirmer le diagnostic par une analyse histologique d’une lésion cutanée évocatrice de lupus.
En cas de suspicion d’atteinte cardiaque ou vasculaire (veine ou artère), il faut effectuer une échographie cardiaque pour rechercher une lésion des valves et de la paroi musculaire. Il peut être nécessaire de demander un doppler ou une angiographie pour rechercher une phlébite.
En cas d’atteinte rénale, il faut absolument réaliser une biopsie rénale (sous anesthésie locale) pour savoir quelle est la sévérité de l’atteinte du rein ce qui permettra d’ajuster le traitement.
En cas d’atteinte neurologique, il faut explorer le cerveau par un examen IRM et/ou analyser le liquide qui circule au sein du cerveau (par une ponction lombaire) qu’on appelle le liquide céphalo-rachidien.
Une atteinte trop sévère des cellules sanguines (cytopénie) peut justifier d’une étude de la moelle que l’on aspirera dans le sternum sous anesthésie locale (myélogramme).
Les radiographies et une échographie avec doppler ou une IRM, sont nécessaires en cas d’arthrite ou de douleurs osseuses.
Etant donné la variabilité des atteintes dans le lupus, cette liste n’est pas exhaustive, car elle dépend de l’expression de la maladie chaque individu qui peut exprimer sa maladie différemment à un moment donné de la vie du malade.
Est-ce que le lupus peut être responsable de la fatigue ?
La fatigue est fréquente au cours du lupus et concernerait 9 malades sur 10. Sa cause est variable et pas toujours bien identifiée. La fatigue est souvent plus marquée au moment de l’automne et de l’hiver.
La fatigue est souvent en rapport avec l’activité de la maladie. Les douleurs articulaires ou musculaires, souvent nocturnes, et l’angoisse légitime sont souvent responsables de troubles du sommeil et sont directement liées à la maladie. Néanmoins, la fatigue peut persister malgré un bon contrôle de la maladie, ce qui suggère l’existence d’autres facteurs intriqués. Des problèmes hormonaux peuvent ainsi être évoqués puisque la fatigue survient plutôt en 2e partie du cycle, à la veille des règles. La fatigue peut aussi être secondaire à un problème de la thyroïde qui est d’origine auto-immune.
La fatigue peut aussi être la conséquence d’un stress excessif, mais il ne faut pas oublier d’évoquer une insuffisance en corticoïdes consécutive à l’arrêt d’un traitement corticoïde prolongé (qui a pu freiner le fonctionnement des glandes surrénales). En cas d’insuffisance surrénale, la fatigue régressera avec la supplémentation en hydrocortisone.
Le lupus est-il responsable de douleurs chroniques ?
Les douleurs articulaires liées aux arthralgies et aux arthrites ont un caractère articulaire net avec un horaire inflammatoire. Elles sont généralement soulagées par les anti-inflammatoires et les immuno-modulateurs. Mais, chez certains malades, les douleurs sont plus diffuses et associées à une grande fatigue et à des troubles de la concentration, alors même que l’activité de la maladie est réduite.
En l’absence de toute évolutivité de la maladie lupique, il faut aussi évoquer un « trouble » du fonctionnement des voies de la douleur dans le cerveau. Ce dérèglement est parfois appelé « fibromyalgie ». Une fibromyalgie associée à un lupus n’expose à aucun risque particulier d’atteinte ou de destruction d’un organe, mais les douleurs ressenties par le patient sont très pénibles, alors même que les médicaments habituels contre la douleur ne sont pas efficaces. Il est important de ne pas augmenter le traitement par la cortisone ou les immunosuppresseurs pour ce type de douleurs. En revanche, l’utilisation de médicaments qui sont prescrits dans la dépression ou l’épilepsie peut avoir un effet antidouleur.
Enfin, il faut se rappeler que les douleurs peuvent être en rapport avec un arrêt trop brutal des corticoïdes chez un malade qui en a pris pendant des années. Dans ce cas, l’organisme ne produit pas assez de corticoïdes par les surrénales et le médecin traitant devra rapidement en prescrire pour éviter tout risque d’insuffisance surrénale aiguë.
Le lupus peut-il provoquer une sécheresse de la bouche ou des yeux ?
Un « syndrome sec » est assez fréquent au cours du lupus et près d’1/3 des malades souffrant de lupus se plaignent d’une sécheresse de la bouche et/ou des yeux. Cette sécheresse est liée à une inflammation d’origine auto-immune des glandes qui produisent la salive (glandes salivaires) ou les larmes (glandes lacrymales). D’autres glandes peuvent être touchées (pancréas, estomac, intestin, vagin,…) et être à l’origine d’autres complications (troubles de la digestion, constipation, dyspareunie…). Ce syndrome sec auto-immun, appelé syndrome de Gougerot-Sjögren, peut-être associé à un lupus et à d’autres maladies auto-immunes.
Le lupus est-il responsable de la chute des cheveux ?
Une chute des cheveux (en terme médical « alopécie »), diffuse ou localisée, peut se produire lors d’une poussée de lupus. Elle est alors un signe d’évolutivité de la maladie. Cette tendance à la chute des cheveux n’est cependant pas constante et s’estompe généralement à distance entre les poussées, lorsque la maladie est stabilisée.
i la chute de cheveux survient en dehors d’une poussée du lupus, il faut rechercher une autre cause qui peut être : un médicament, une carence en fer, une carence en vitamines, un excès de testostérone (hyperandrogénie (excès de testostérone) ou, comme dans la population normale, l’usage d’un shampoing trop agressif ou l’application trop fréquente de teintures. Des situations de stress peuvent aussi favoriser la chute de cheveux. Enfin, il faut toujours éliminer une atteinte thyroïdienne.
Comment évolue le lupus ?
Sans traitement, le lupus systémique évolue par poussées évolutives de la maladie, alternant avec des phases de calme relatif. Malheureusement, cette évolution « naturelle » est susceptible d’aboutir, dans le cas de poussées évolutives sévères, à des dommages irréversibles dans les organes concernés par la maladie : séquelles articulaires, cutanés, musculaires, rénales, neurologiques…
Sous traitement, l’évolution habituelle du lupus érythémateux systémique se fait vers la rémission avec disparition des signes cliniques et amélioration de certains signes biologiques, comme le taux des anticorps anti-ADN. L’activité de la maladie est réduite à son minimum, mais la maladie n’est pas guérie. En particulier, les anticorps antinucléaires restent souvent présents, même lorsque le lupus est complètement contrôlé.
L’objectif est de maintenir la rémission avec un traitement qui sera réduit très progressivement à la dose minimale qui permet de garder le contrôle de la maladie (traitement minimum efficace). Si le traitement est bien suivi, sans interruption intempestive, le risque de reprise d’activité de la maladie (poussées) est plus faible, et les poussées évolutives sont plus rares. Par ailleurs, lors de chaque poussée, un traitement précoce et intensif d’emblée permet aussi de limiter considérablement le risque des séquelles.
Quels sont les principes du traitement du lupus ?
Le lupus est une maladie chronique, c’est-à-dire que l’on ne peut pas la guérir complètement. Avec les traitements dont nous disposons, il est cependant possible d’obtenir de longues périodes où la maladie n’est plus apparente sous traitement : on parle alors de « rémission ». C’est ce que les médecins cherchent à obtenir en ajustant constamment l’intensité du traitement (nombre de médicaments et doses des médicaments). Pour être plus efficaces, les traitements vont combiner différents types de médicaments, à différents dosages, en s’adaptant en permanence au niveau d’activité de la maladie, et ce tout au long de la vie du patient. La principale difficulté pour le médecin est d’avoir les bons indicateurs d’activité en temps utile. La principale difficulté pour le malade est de dépister les signes qui doivent faire évoquer un changement d’activité de la maladie et de suivre le traitement tout au long de sa vie.
Le premier temps du traitement vise à contrôler le plus rapidement possible l’activité de la maladie pour préserver les organes vitaux des poussées graves. Il s’agit de contrôler très vite l’inflammation et de diminuer rapidement l’activation du système immunitaire.
Le deuxième temps du traitement, une fois la rémission obtenue, vise à contrôler la maladie avec les doses les plus faibles possibles du traitement. Il s’agit de prévenir la réactivation de la maladie lupique et les atteintes d’autres organes qui en découlent. En cas de syndrome des anti-phospholipides, l’enjeu est aussi d’empêcher l’apparition de caillots dans le sang. Enfin, il faut aussi limiter à long terme les séquelles du lupus et les effets secondaires des traitements que l’on est obligé d’utiliser dans les phases très actives de la maladie.
Enfin, il faut aussi soulager le malade avec des médicaments contre l’inflammation et la douleur (médicaments symptomatiques).
Les traitements ayant une action sur l’évolution de la maladie sont appelés traitements de fond et ils sont classés en 4 catégories :
• La cortisone (corticoïde) est un médicament qui permet à la fois de lutter contre l’inflammation au cours d’une poussée et qui module l’activité de certaines cellules de l’immunité. Il s’agit donc d’un traitement de fond qui fait partie des médicaments du traitement sur le long terme.
• Les immunomodulateurs et immunosuppresseurs « classiques » sont, en premier lieu, les antipaludéens de synthèse (ou antimalariques) : l’hydroxychloroquine essentiellement qui agit à plusieurs niveaux de la réponse immunitaire pour mieux contrôler la maladie. Ce sont aussi le méthotrexate, l’azathioprine, le cyclophosphamide, l’acide mycophénolique. Le méthotrexate est surtout utilisé dans les atteintes sévères des articulations, et les autres dans les atteintes sévères rénales, ou neurologiques.
• De « nouveaux » immunomodulateurs, appelés également « biomédicaments » ou biothérapies, agissent sur une cible « biologique » très précise qui intervient à un niveau clé dans les mécanismes de la maladie. Par exemple, il a été démontré dans le lupus le rôle majeur des lymphocytes B, et des biothérapies, comme le rituximab, sont capables de neutraliser leur fonction immunitaire. De nombreuses molécules dirigées contre des cellules ou des constituants de l’immunité (comme les cytokines) sont en cours d’évaluation dans le lupus : le belimumab est un anticorps dirigé contre une protéine de l’inflammation, le BAFF, qui augmente l’activité des lymphocytes B, ceux-ci ayant un rôle clé dans la maladie.
Comment éviter les complications des corticoïdes ?
Pour éviter les complications des corticoïdes à forte dose, comme une hypertension artérielle, un régime sans sel est parfois proposé. En fait, le régime sans sel strict n’est important qu’en cas de fortes doses de cortisone (au-delà de 15 mg/j). Un régime « peu salé » s’avère la plupart du temps suffisant. Dans les autres cas (les plus fréquents), aucune restriction de sel n’est nécessaire.
Comme la prise de cortisone (« corticothérapie ») fait perdre du potassium, un apport de potassium par la bouche est nécessaire durant la période où la cortisone est prescrite à dose moyenne ou forte (en général au-delà de 15 mg/j), mais cela peut aussi dépendre des traitements associés.
Pour éviter la prise de poids, et d’éventuels troubles métaboliques (comme le diabète), il est habituel de proposer un régime pauvre en graisses et en sucres.
Pour prévenir l’ostéoporose, un régime riche en calcium et en vitamine D est conseillé. Les apports quotidiens recommandés en calcium seront la plupart du temps couverts par une alimentation équilibrée (avec au moins 2 à 3 laitages par jour), sinon une prescription complémentaire de calcium sera nécessaire. La pratique régulière d’une activité physique adaptée est également nécessaire, afin de stimuler les cellules osseuses et de tonifier les muscles. Enfin, pour lutter contre l’ostéoporose, en particulier après la ménopause, certains médicaments anti-ostéoporotiques, appelés bisphosphonates, peuvent être utiles et prescrits dès la mise en route d’un traitement par cortisone à dose au-delà de 7,5 mg/jour.
Il faut consulter rapidement son médecin en cas de fièvre, ou de symptômes évoquant une infection (toux, brûlures urinaires, éruption ...), et se souvenir qu’une petite lésion anodine peut s’aggraver à cause du traitement que l’on prend, si elle est négligée. Les soins habituels d’hygiène corporelle (brossage des dents, toilette intime) doivent être soigneux, mais attention aux soins de pédicure trop « agressifs », car ils peuvent favoriser les infections.
Le carnet vaccinal doit être à jour et, s’il y a un traitement immunosuppresseur associé, la vaccination anti-pneumococcique est recommandée.
Pour éviter l’athérosclérose accélérée, il n’y a pas de mesure spécifique. Il faut se souvenir que ce risque est d’autant plus important que la corticothérapie s’associera à d’autres facteurs de risque cardiovasculaire, comme l’obésité, l’hypercholestérolémie et/ou la ménopause.
Comment traiter un syndrome de Raynaud ?
La principale recommandation est de protéger les mains et les pieds du froid. Il faut donc s’habiller chaudement. Il faut garder la tête et le cou au chaud car ce sont des sources de perte de la chaleur du corps. Il faut se méfier de l’air conditionné, car un changement rapide de la température peut déclencher une crise. Il faut surtout porter des gants mais les doigts et les mains ne doivent pas être à l’étroit et se chausser avec des chaussures chaudes et larges, de préférence en cuir, afin de mettre des chaussettes chaudes. On peut avoir recours à un apport de chaleur dans certaines situations, à condition que la chaleur dégagée ne soit pas excessive (chaufferettes, chauffe-pieds électrique, couverture électrique ...).
Le contact avec l’eau froide est un facteur fréquent de déclenchement des crises de syndrome de Raynaud et il faut faire la vaisselle et le nettoyage (ménage, légumes,…) à l’eau chaude. Il faut éviter la prise d’objets froids sans protection des mains (produits surgelés, volant de la voiture le matin, poignée de porte extérieure,…). Il est aussi conseillé d’appliquer fréquemment des crèmes hydratantes sur les mains pour prévenir les blessures et fissures de la peau qui sont favorisées par la mauvaise circulation.
En cas de travail avec des outils mécaniques entraînant des vibrations, il vaut mieux tenir l’outil d’une prise légère, et sans crispation, ce qui évite trop de secousses pour les mains et les bras.
Enfin, il est très important d’arrêter de fumer car la nicotine abîme les vaisseaux sanguins et réduit la circulation du sang dans les extrémités.
Pour la majorité des malades, les médicaments ne sont pas utiles. Parfois, lorsque les crises de Raynaud sont sévères et invalidantes, le médecin peut être amené à prescrire des médicaments de type vasodilatateurs, qui favorisent la circulation sanguine dans les doigts et les orteils en augmentant l’ouverture des vaisseaux sanguins.
Peut-on guérir du lupus ?
Avec les médicaments dont nous disposons, on ne peut pas obtenir de guérison de la maladie lupique, c'est-à-dire une disparition définitive de la maladie même après arrêt des médicaments. Toutefois, certains patients peuvent avoir des rémissions très prolongées (c’est-à-dire une disparition de tous les signes de la maladie) avec un traitement qui a été réduit à son minimum.
Le lupus est une maladie chronique, mais dont les signes peuvent être soulagés efficacement par un traitement adapté. Certains médicaments permettent également de diminuer le risque d’apparition d’une poussée évolutive ou d’une complication de la maladie lupique. L’important pour le malade est de prendre ces médicaments à une dose adaptée (qui peut être variable) et pendant longtemps : c’est ce qui permettra d’éviter une rechute. L’activité du lupus a toutefois tendance à diminuer après la ménopause et le risque de rechute va aussi diminuer.
Comment vivre avec un lupus ?
Les traitements dont nous disposons actuellement permettent de mettre le lupus en rémission dans la plupart des cas, mais ils doivent être pris sur de très longues périodes. Dans ce contexte, la maladie a des conséquences sur la vie quotidienne du patient qui doit adapter certaines de ses activités et adopter certains réflexes pour préserver au mieux ses chances de rester en rémission ou pour ne pas avoir des complications.
En cas de prise de cortisone, il faut une bonne hygiène alimentaire pour réduire le risque de retentissement cardiaque, osseux ou sur le métabolisme des sucres. Certains régimes ont été mis en avant pour mieux contrôler le lupus, mais leur efficacité n’a pas encore été prouvée. L’essentiel est de conserver un bon équilibre alimentaire pour éviter de provoquer des carences notamment en vitamines et en calcium.
L’arrêt du tabac est indispensable pour obtenir une moindre évolutivité de la maladie sur le long terme. En effet, le tabagisme est susceptible de diminuer l’efficacité des antipaludéens de synthèse et il accélère le risque d’athérosclérose qui constitue la première complication à long terme du lupus, avec le risque infectieux.
La pratique d’une activité physique ou sportive entretient la force musculaire qui peut être perturbée par certains traitements, notamment la cortisone, et elle permet de lutter contre les maladies cardiovasculaires. Elle contribue également à réguler le poids. Pendant une poussée, il est déconseillé de faire une activité physique mais, une fois la rémission obtenue, sa reprise est recommandée.
Pour tous les malades souffrant de lupus, l’exposition au soleil est fortement déconseillée car elle risque d’aggraver la maladie, même pour ceux qui n’ont jamais eu de signes cutanés.
Les bains de soleil sont à proscrire et il est nécessaire d’avoir une protection efficace de la peau lorsque le rayonnement solaire est fort, comme en bord de mer ou en haute montagne (la neige et l’eau reflètent les rayons ultraviolets du soleil). Il faut savoir que les vêtements blancs ou un parasol laissent passer les rayons du soleil. Les sorties aux heures où le rayonnement (UV) est maximal, soit entre 12 h 00 et 16 h 00, sont des sorties à risque pour le malade souffrant de lupus.
En cas de soleil, le malade lupique doit privilégier des vêtements à manches longues et les pantalons au tissage serré (coton, jean) et aux couleurs foncées. Il existe également sur le marché des vêtements de sport anti-UV. Il faut appliquer sur le visage et les mains des crèmes solaires avec un indice de protection supérieur à 50, protégeant des rayons UVA et UVB. Pour être efficace, l’écran solaire doit être appliqué toutes les 2 heures, en particulier après chaque baignade, même sous un temps nuageux (près de 80 % des rayons UVB traversent les nuages, la brume et le brouillard), et même sous un parasol.
Le port d’un chapeau à large bord ou d’une casquette à visière est aussi recommandé.
Les autobronzants sont autorisés, mais ils ne protègent pas du soleil.
Peut-on se faire opérer quand on a un lupus ?
Une opération est bien sûr toujours possible à la condition d’informer le chirurgien et l’anesthésiste de votre maladie et des traitements pris.
En particulier, le syndrome des anti-phospholipides doit faire l’objet d’une prise en charge particulière, avec un ajustement des traitements anticoagulants.
Du fait du traitement immunosuppresseur et la prise de cortisone depuis longtemps, il sera nécessaire de prévenir la survenue d’une infection dans la période post-opératoire immédiate.
Peut-on se vacciner quand on a un lupus ?
Les malades souffrant de lupus ont un risque infectieux accru et la vaccination est un élément important de la protection des malades contre les infections. Les vaccinations usuelles ne sont pas associées à une plus grande fréquence de poussées de la maladie lupique, en revanche, en cas de traitement par immunosuppresseurs ou corticoïde au long cours, les vaccins vivants atténués sont contre-indiqués (BCG, fièvre jaune, polio orale, rougeole, rubéole, oreillons). À l’inverse, le vaccin anti-pneumococcique est fortement recommandé en cas de traitement par immunosuppresseur.
Peut-on faire du sport quand on a un lupus ?
Le sport, ou une activité physique, peut être pratiqué le plus souvent possible, mais il faut être prudent en cas de traitement anticoagulant ou de baisse du taux de plaquettes.
La pratique régulière du sport sans excès entretient la force musculaire, qui peut être altérée par certains traitements, comme la cortisone. Le sport permet de lutter contre les maladies cardiovasculaires, qui sont plus fréquentes au cours du lupus. Le sport, enfin, contribue à contrôler le poids.
Les situations où le sport doit être évité au cours du lupus sont rares. En cas de traitement anticoagulant ou de baisse du taux de plaquettes, il existe un risque de saignement en cas de blessure s’il y a pratique d’un sport violent (on déconseille par exemple d’escalade, les sports de vitesse).
Lorsque le lupus est en poussée, le sport doit être évité, mais il est possible de pratiquer la marche ou la gymnastique si des douleurs articulaires ou musculaires n’apparaissent pas. Les vraies contre-indications sont très exceptionnelles : polyarthrite sévère en poussée, atteinte cardiaque ou pulmonaire.
Quelle contraception peut-on prendre au cours du lupus ?
Une vie sexuelle tout à fait normale est possible au cours du lupus. Il faut en parler au médecin pour surmonter certaines craintes. Le principal problème est celui de la contraception qui ne peut pas être basée sur les contraceptifs traditionnels, comme les estro-progestatifs. Ceux-ci font courir un risque d’aggravation de la maladie, en raison de la présence des estrogènes. Le médecin conseillera donc une éventuelle contraception basée sur la contraception locale et dans certaines circonstances sur les progestatifs seuls.
En cas de syndrome sec associé, il sera nécessaire de prévoir des lubrifiants vaginaux pour éviter les douleurs liées à la sécheresse vaginale (dyspareunie).
Peut-on avoir des enfants au cours d’un lupus ?
En dehors des phases où la maladie est mal contrôlée, la grossesse est possible au cours d’un lupus qui est correctement suivi et traité et les grossesses se passent le plus souvent bien. Mais il est nécessaire de programmer la grossesse au cours des phases où la maladie est inactive : le lupus doit être en rémission depuis au moins 6 à 12 mois. Il faudra ajuster le traitement et augmenter la surveillance afin de vérifier que le lupus ne redevient pas actif et incontrôlé. Il faut aussi prévenir la survenue des caillots en prenant de l’aspirine et/ou une anticoagulation et, en particulier, en cas de syndrome des anticorps anti-phospholipides.
Dans certains cas, notamment en cas d’insuffisance rénale, les risques de la grossesse seront tels que le médecin pourra déconseiller la grossesse. En cas de prise de fortes doses de cyclophosphamide, par exemple, en cas d’atteinte rénale ou cérébrale, la grossesse ne sera pas possible en raison d’une ménopause prématurée.
Peut-on travailler et avoir un métier ?
Le lupus est une maladie chronique qui ne perturbe pas le travail pendant la rémission. Mais, si la maladie est très sévère ou mal traitée, les poussées évolutives peuvent nécessiter un arrêt de travail.
Il faut bien évidemment éviter les activités professionnelles de plein air, car l’exposition solaire ferait courir un risque de poussées de la maladie. Il en est de même pour les activités professionnelles où il y a beaucoup de stress. En cas de traitement anticoagulant, il convient d’éviter les activités professionnelles à risque de traumatisme.
Mais, le principal problème des malades reste la fatigue et il faut pouvoir prévoir des temps de repos. Lorsque cette fatigue n’est pas permanente, un travail est largement possible et préférable, afin de favoriser un bon équilibre de vie et l’insertion socio-professionnelle.
Peut-on fumer quand on a un lupus ?
L’arrêt du tabac est indispensable quand on souffre d’un lupus. Le tabac est en effet un facteur de risque de plus grande activité dans le lupus et les maladies auto-immunes. Le tabac peut même diminuer l’efficacité des traitements comme les antipaludéens de synthèse, même s’il n’en modifie pas les taux dans le sang.
Même si cette relation négative entre lupus et tabac est moins forte que celle qui a été établie dans d’autres maladies auto-immunes comme la polyarthrite rhumatoïde, l’arrêt du tabac est recommandé, d’autant qu’il fait courir un risque d’athérosclérose accélérée. Or, l’athérosclérose constitue la première complication à long terme du lupus, avec le risque infectieux.
Le tabac est nocif même s’il est passif et il faut éviter les zones où quelqu’un est susceptible de fumer.
Peut-on prendre l’avion quand on a un lupus ?
Le lupus ne contre-indique pas les voyages, sous réserve de se protéger suffisamment du soleil en cas de destination vers un pays ensoleillé et d’emporter suffisamment de médicaments. Tous les modes de transport sont possibles, sauf dans de très rares situations, par exemple en cas de risque de thrombose ou quand le lupus se complique d’hypertension des artères pulmonaires (hypertension artérielle pulmonaire ou HTAP).
Les vols long-courriers augmentent les risques de phlébites. Le port de chaussettes de contention diminue ce risque. Pour les patients, qui sont sous anticoagulant parce qu’ils ont déjà fait une phlébite, ou une embolie pulmonaire, ils sont protégés par leur traitement anticoagulant, si celui-ci est bien équilibré. Pour les patients lupiques qui ont dans le sang des anticorps antiphospholipides (anticardiolipine ou antiprothrombinase), il peut être recommandé, dans certains cas, de faire une injection sous-cutanée d’héparine de bas poids moléculaire une heure avant le départ de l’avion.
L’HTAP entraîne une gêne respiratoire, en particulier à l’effort ou en cas de quantité réduite en oxygène (comme en altitude). Les avions des grandes lignes sont tous pressurisés et il n’y a en général pas de problème, mais certains modèles donnent des pressurisations qui peuvent être basses.
Peut-on aller dans un pays tropical quand on a un lupus ?
Les pays tropicaux exposent à deux risques importants pour le lupus, le soleil avec son risque de poussée lupique et les infections, en particulier la fièvre jaune et le paludisme.
La protection contre le soleil est très importante et doit être faite. Il faut bien sûr partir avec suffisamment de traitement.
Les vaccinations doivent être à jour et le principal problème est la vaccination contre la fièvre jaune qui est un vaccin à virus vivant et qui ne peut être réalisée que si le malade ne prend pas d’immunosuppresseurs.
Concernant la prophylaxie contre le paludisme, une consultation spécialisée est nécessaire pour évaluer l’exposition au parasite et le choix de la prophylaxie en fonction du pays et du mode de vie sur place (séjour urbain ou rural, en saison sèche ou des pluies,…).
Dans tous les cas, la première mesure de prévention concernant le paludisme reste la protection contre les piqûres de moustiques : par les répulsifs, par le port de manches longues et d’un pantalon le soir et par le recours systématique à une moustiquaire pour dormir. Ceci aura, d’autre part, l’avantage de protéger contre les autres infections qui peuvent être transmises par les moustiques (comme la dengue).
Le parasite provoquant le paludisme est de plus en plus souvent résistant aux antipaludéens et les différents pays ont été classés par l’OMS vis-à-vis de la résistance aux antipaludéens, et notamment à la chloroquine. Cette classification répartit les pays en 3 zones de risque, de 1 à 3 (Zone 1 : pas de résistance à la chloroquine, Zone 2 : résistance intermédiaire et Zone 3 : pays de forte résistance).
En cas de voyage en Zone 1, le traitement recommandé est le sulfate de chloroquine (Nivaquine®), si ce traitement est déjà prescrit, il peut être poursuivi à la même posologie que dans le lupus et il sera suffisant. Si le traitement prescrit dans le lupus est l’hydroxychloroquine (Plaquenil®), les données sur la protection antipalustre conférée sont peu nombreuses, mais son utilisation en tant que chimioprophylaxie traitement antipaludéen est possible, à la même posologie que celle qui est réalisée dans le lupus.
Peu de pays sont actuellement classés en Zone 1, car la résistance du paludisme est devenue très fréquente et va en augmentant. En cas de voyage en Zone 2 ou en Zone 3 (zones qui concernent la plupart des pays d’Afrique et d’Asie), un traitement adapté au niveau de résistance doit être instauré parallèlement au traitement contre le lupus. L’avis d’un médecin spécialisé est impératif afin de juger de la possibilité ou non de prescrire ces prophylaxies médicaments sans risque, en fonction d’éventuelles contre-indications (possible complications neuropsychiatrique ou photosensibilité) ou interactions avec le traitement du lupus : certaines molécules sont donc à éviter en cas de lupus systémique. Certaines associations antipaludéennes de Zone 2 ou 3 contiennent déjà un antipaludéen, mais ces prophylaxies peuvent être associées au traitement habituel du lupus car leur prescription est généralement limitée dans le temps.
Le lupus en France
Selon les estimations, il existerait entre 20 000 et 40 000 cas de lupus en France. Cette maladie touche surtout les femmes entre 15 et 45 ans, et celles-ci représentent donc près de 90 % des cas.
Les liens du lupus
Le site du centre national de référence sur le lupus
Le site de l’Association Lupus France
Les liens internes à Pourquoi Docteur
Les pompiers de Ground Zero ont plus de maladies auto-immunes
Lupus : le traitement hormonal substitutif doublerait le risque
Les vidéos du lupus sur Youtube













Commentaires